- 所有服务
- 生命科学服务平台
- 诊断原料开发服务平台
- 抗体药物研发服务平台
等温滴定量热(ITC)实验服务
- 产品信息(Product Details)
等温滴定量热法用来测定各生物分子之间的反应。该方法可测定结合亲和力、化学计量以及溶液中结合反应的熵和焓,无需使用标记。发生结合时,热不是被吸收就是被释放,这是在配体被逐渐滴定到包含目标生物分子的样品池过程中通过灵敏量热计而测得。
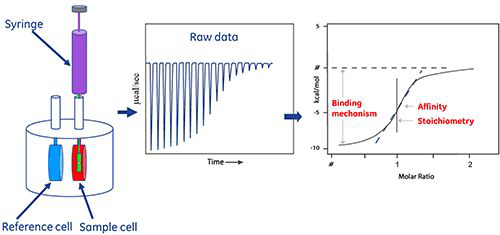
图为原理示意
热核心
进行测量
参比池和样品池被设定到所需的实验温度。将配体装入一个非常精确的注射装置上的注射器中。将注射装置插入包含目标蛋白质的样品池中。将一系列小份配体试样注入到蛋白质溶液中。如果有配体与蛋白质结合,则可检测到并测出几百万分之一摄氏度的热量变化。进行第一次注射时,微量热计测量被释放的所有热量,直到结合反应达到平衡。 测得的热量与结合量成正比。
结果和数据分析
在下面的示例中,反应是放热的,这就意味着样品池温度高于参比池并由此导致信号出现下行波峰。随着两个池的温度恢复到同一水平,信号也回到其起点。将第二小份配体试样注入到样品池中,同样,微量热计补偿所检测到小幅热量变化。配体与蛋白质之间的摩尔比随着一系列配体试样的注入而逐渐增加。蛋白质越来越饱和,配体结合的次数越来越少,并且热量变化开始减小,直到样品池中的配体数量相对于蛋白质而言最终表现出过量为止,从而使反应朝饱和的方向进行。

图为原理示意
然后对每个峰的面积进行积分,并以配体与蛋白质的摩尔比作为横坐标进行绘图。由此得出的等温线可拟合至导出亲和力 (KD) 的结合模型。结合等温线中心的摩尔比即为反应化学计量。下图给出了 1:1 结合反应的示例图。
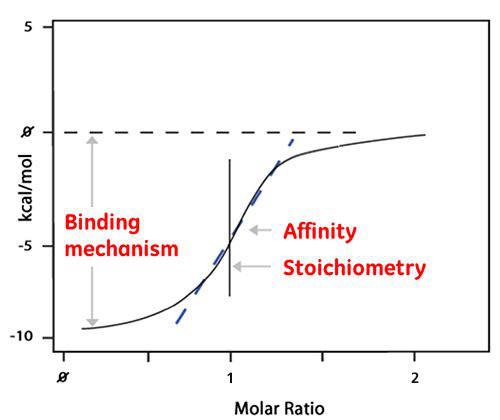
焓 (ΔH) 也可通过等温线直接导出,它表示每摩尔结合配体所释放的热量。这就意味着一次 ITC 实验就可提供丰富的结合反应信息,有助于理解相互作用的性质并探索热力学驱动因素。
ITC 广泛用于药物发现和开发领域的以下方面:
量化结合亲和力
候选药物的选择与优化
测定热力学特性和活性浓度
作用机制表征
在小分子药物发现过程中确认预期结合靶标
测定结合特异性和化学计量
验证从苗头化合物到先导化合物演化过程中的 IC50 值和 EC50 值
酶动力学测定