在全蛋白质组水平检测PROTAC分子on target/off target,是该类药物开发过 程中的关键环节。Proteolysis Targeting Chimeric (PROTAC)技术核心是发展能与靶蛋白结合并招募降解酶的双功能分子,利用 该分子招募泛素化酶靠近靶蛋白,从而 使其泛素化降解,该技术可用于治疗多种疾病。
PROTAC的优势
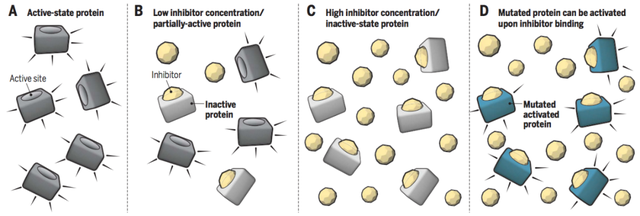
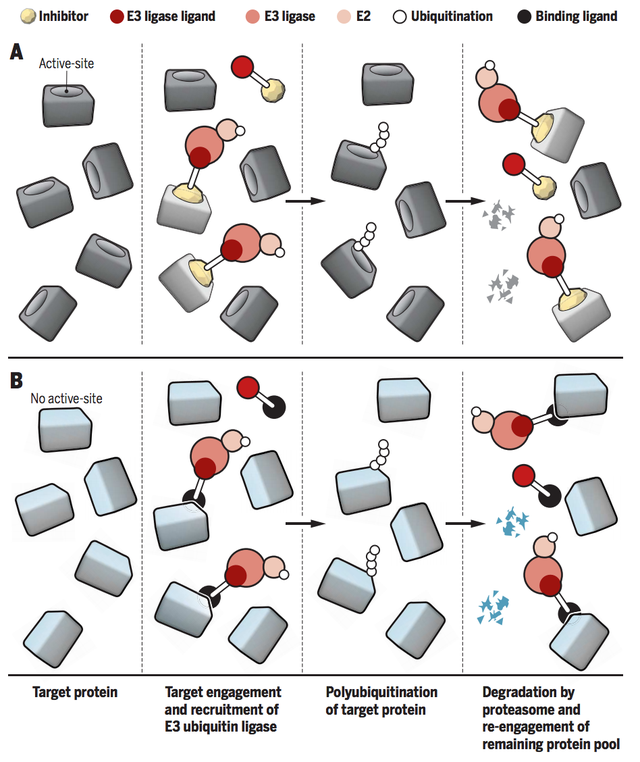
(1)作用范围更广、活性更高、可靶向“不可成药”靶点传统的小分子和抗体等都是通过“占据驱动”的作用模式抑制靶蛋白的功能发挥治疗疾病的作用,这种作用模式需要抑制剂或单抗具备较高的浓度才能够占据靶点的活性位点,阻断下游信号通路的转导。而PROTAC是“事件驱动”,不是影响蛋白的功能,而是介导致病靶蛋白被降解。只要PROTAC介导三元复合物的形成并给靶蛋白打上泛素化的标签,理论上是可以循环反复使用的,因此催化剂量即可发挥作用。而且PROTAC对于没有活性位点的蛋白,如支架蛋白等,只要能够产生结合作用就可以诱导相关蛋白被降解,可以大大提高靶点的范围。
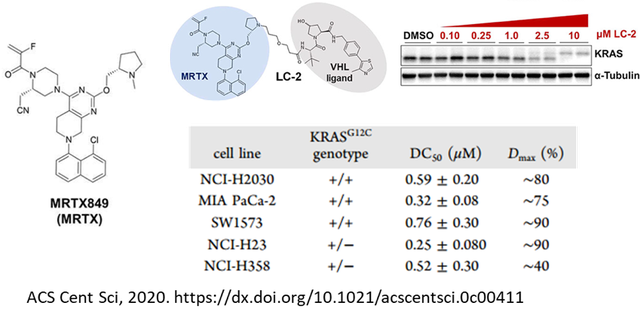
与传统小分子抑制剂相比,PROTAC在某些靶点上可实现小分子难以实现的选择性。例如,多靶点酪氨酸激酶抑制剂Foretinib可以结合130多种激酶,Crews等人将其作为结合靶蛋白的配体,分别连接E3连接酶VHL(von Hippel-Lindau)和CRBN(cereblon)的配体得到相应的PROTAC,结果显示连接VHL和CRBN的PROTAC只能分别降解36和62种蛋白,而只有12种蛋白才能被这两种PROTAC降解。另外一项Gray课题组的研究也证明了PROTAC可以实现靶点的选择性。2,4-二氨基嘧啶骨架是激酶抑制剂的常见骨架,EGFR、ALK、CDK、Jak等激酶的抑制剂都有用到其作为母核。但是该骨架形成的药物分子大多都比较“脏”,也就是靶点选择性比较差,经常对其他很多激酶都有很强的抑制活性,开发过程中off target的脱靶效应常常成为毒副作用的主要来源,影响新药开发的成功率。Gray课题组基于该骨架合成的PROTAC虽然能够结合190多种激酶,但是细胞实验中只能降解12和22种激酶,大大提高了靶点的选择性。由此可见,合理的药物设计加之反复迭代优化,选择性更高、活性更好、安全性更佳的PROTAC分子很有可能被发现。PROTAC技术不仅可以实现小分子抑制剂难以做到的选择性,在提高活性方面也具有非常显著的优势。以PROTAC技术应用最早的靶点BET(BRD2/3/4)为例,秦冲等人发现的QCA570在细胞抗增殖活性方面表现出了明显优于JQ1等抑制剂的能力,JQ1等抑制剂的活性大都在纳摩尔级水平,而QCA570的活性提高了三个数量级,达到了惊人的皮摩尔级水平。基于出色的体外细胞抗增殖活性,降解剂在体内也表现出了强效抗肿瘤活性,而且呈现出给药剂量低和给药频次也低的特点。这说明在类似BET等靶点中,PROTAC具有明显的优势。但是一直未见有针对该靶点的降解剂进入临床,具体原因不明。
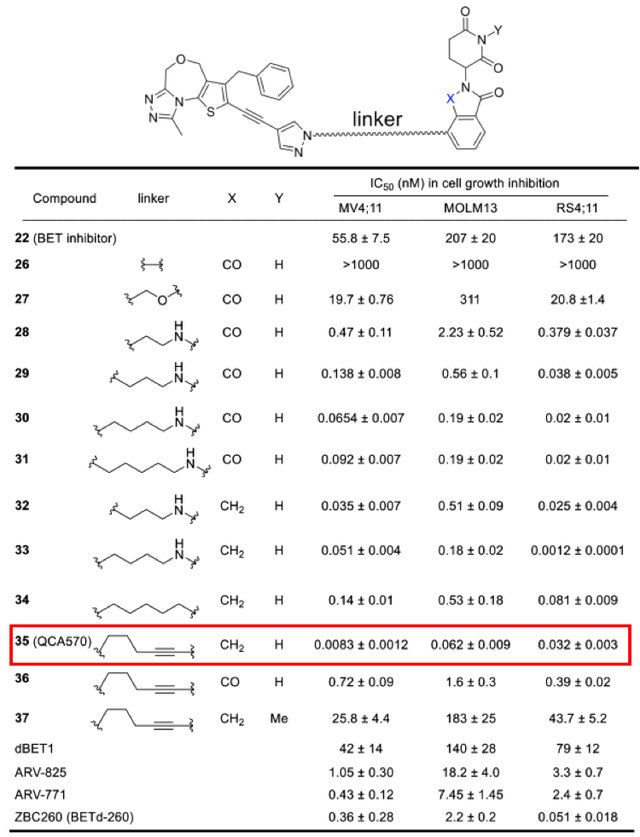
(3)克服药物的耐药性
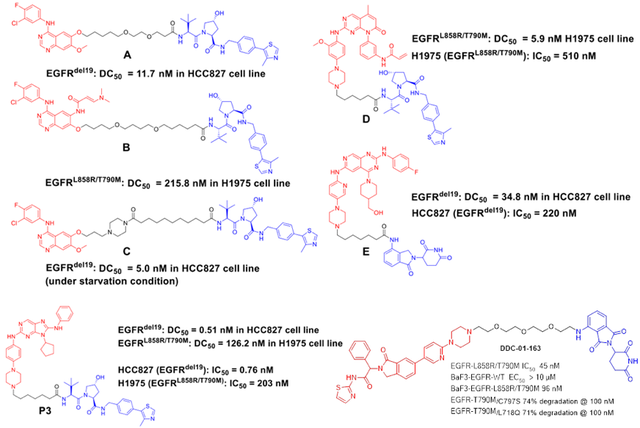
小分子抑制剂或拮抗剂在临床用药过程中,不可避免的都会发生获得性耐药。比如EGFR-T790M和C797S耐药等。虽然可以通过开发新一代的抑制剂,如第三代和第四代EGFR来解决耐药问题,但是随着新一代药物的使用,新的耐药也会随之出现。PROTAC技术在克服耐药方面已经显现出了一定的优势。Crews、Jian Jin、张三奇、丁克和Gray等课题组都有相关EGFR-PROTACs的研究,旨在通过蛋白降解途径克服耐药突变或找寻突破抑制剂的蛋白降解疗法。可以看出,第一、二、三、四代抑制剂作为结合靶蛋白EGFR的配体,都有被应用到PROTAC的设计中。其中,Gray课题组将变构抑制剂也应用到了PROTAC当中,并取得了不错的效果,能够选择性的降解不同的EGFR突变体,而规避对野生型的降解。体外抗细胞增殖活性也进一步验证了这种选择性。
武汉研锦生物面向制药企业、医院和科研院所,可提供药物钓靶质谱鉴定分析和检测分子间亲和力服务。包括药物高通量虚拟筛选、分子对接分析、 动力学模拟、细胞原位垂钓靶点蛋白等,以及SPR、MST、DSF、BLI、ITC等亲和力检测服务和Olink 高灵敏超微量多指标蛋白芯片检测服务。涉及小分子药、生物药、中药、天然药物等多种新药类型,为您提供优质的药物钓靶和活性检测服务。电话 | 微信:张工15337192895/18963979811Yangenebio提供Biacore SPR、BLI、MST、ITC、DSF蛋白稳定性分析等检测,天然药物垂钓靶点服务;依托SPR-Selex垂钓细胞裂解液、核酸文库等筛选靶点检测服务。















